a) 0,8 atm
b) 0,9 atm
c) 1,0 atm
d) 1,2 atm
e) 1,5 atm
79) Um recipiente indilatável e vedado hermeticamente contém um gás em seu interior. Se a temperatura é de 27 oC, a pressão exercida pelo gás é de 1 atm. Considere o gás como ideal. A pressão do gás será de 2 atm, se a temperatura no interior do recipiente for, em oC, igual a:
a) 54
b) 108
c) 300
d) 327
e) 600
80) Certa massa de gás perfeito tem volume Vo, pressão po e temperatura igual a 327 oC. Quando o volume for Vo/2 e a pressão 4po/3, a temperatura, em oC, será igual a:
a) 127
b) 200
c) 427
d) 900
81) Um gás perfeito sofre um processo no qual sua pressão fica constante e sua temperatura passa de 0 oC para 136,5 oC. Nessas condições, o seu volume é:
a) reduzido à metade.
b) duplicado.
c) reduzido a um terço do inicial.
d) triplicado.
e) mantido constante.
82) A figura representa duas isotermas de uma mesma quantidade de gás ideal, correspondentes às temperaturas absolutas T1 e T2.

A razão T1/T2 entre as temperaturas absolutas é:
a) 16
b) 4
c) 1
d) ¼
e) 1/16
83) Uma pessoa fecha com a palma de sua mão a extremidade de uma seringa e com a outra mão puxa o êmbolo até as proximidades da outra extremidade, mantendo a temperatura constante. O gráfico P x V que melhor representa este processo é:
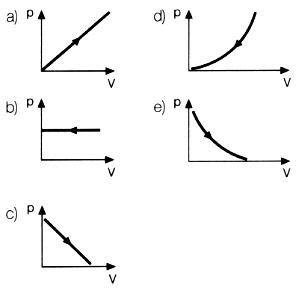
84) 15 litros de uma determinada massa gasosa encontram-se a uma pressão de 8 atm e à temperatura de 30o C. Ao sofrer uma expansão isotérmica, seu volume passa a 20 litros. Qual será a nova pressão?
a) 10 atm
b) 6 atm
c) 8 atm
d) 5 atm
e) É impossível determinar.
85) Nos gráficos abaixo, p é a pressão, V é o volume e T é a temperatura absoluta de um gás perfeito. O gráfico que representa uma transformação isobárica é o da alternativa,

86) Uma certa massa gasosa ideal sofre uma transformação a volume constante, conhecida como lei de Charles. Sua pressão inicial é de uma atmosfera e sua temperatura passa de 400 K para 500 K. A pressão da massa gasosa passa para:
a) 0, 80 atm
b) 1,25 atm
c) 1,50 atm
d) 1,70 atm
e) 1, 80 atm
87) Um tanque rígido, cujo volume é 10 m3, contém ar à pressão atmosférica. Supondo que a temperatura permaneça constante, quantos metros cúbicos adicionais de ar, à pressão atmosférica, deverão ser bombeados para dentro do tanque de modo que a pressão interior se tome dez vezes a pressão atmosférica?
a) 50
b) 70
c) 90
d) 110
e) 130
88) Uma dada massa de gás hélio sofreu uma transformação que a levou de um estado de equilíbrio inicial I, situado no plano pressão x volume, para um estado de equilíbrio final F, do mesmo plano, conforme afigura. Se a temperatura do estado inicial era 100 K, a temperatura do estado final é:

a) 100 K
b) 200 K
c) 400 K
d) 700 K
89) O volume de uma bolha de ar triplica de valor quando ela sobe do fundo à superfície de um lago. Considerando a temperatura da água constante e a pressão atmosférica igual a 1,0.105 N/m2, qual é, aproximadamente, a profundidade do lago? (Considere a densidade da água = 103 kg/m3.)
a) 3 m
b) 10m
c) 20 m
d) 30 m
e) 40 m
90) Uma câmara de gás contém uma massa m de 02 sujeita à pressão p. Mantendo constante a temperatura e duplicando a massa de oxigênio, seu volume aumenta 25%. Portanto, a pressão:
a) aumenta 60%.
b) aumenta 25%.
c) diminui 25%.
d) aumenta 75%.
e) diminui 75%.
Para responder às questões de números 91 e 92 considere as informações abaixo.
Um recipiente rígido contém 0,500 ml de gás perfeito, à temperatura de 27 oC e pressão de 1,2 atm. Esse recipiente é provido de uma válvula que libera gás sempre que a pressão exceder 1,6 atm.
91) A temperatura do gás quando a pressão for igual a 1,5 atm será, em Kelvin, aproximadamente igual a:
a) 2,4. 10^2
b) 3,0. 10^2
c) 3,6. 10^2
d) 3,8. 10^2
e) 4,5. 10^2
92) Sendo a temperatura de 227 oC, a válvula já foi ativada e liberou, no máximo, uma quantidade de gás, em mols, igual a:
a) 0,10
b) 0,15
c) 0,20
d) 0,25
e) 0,30
93) O volume molar de um gás perfeito vale 22,4 litros à temperatura de 0 oC e pressão de 1 atm. O volume do mesmo gás à temperatura de 27 oC e à pressão de 76 cmHg será, em litros:
a) 25,4
b) 22,6
c) 24,6
d) 23,4
e) 26,2
94) O volume ocupado por 2,0 mols de um gás ideal à pressão de 2,0.105 N/m2 e a 27 oC é, em m3:(Dado: R = 8,31 J/mol.K)
a) 4,4.10-3
b) 2,2.10-3
c) 2,5.10-2
d) 2,2.10^1
e) 2,5.10-8
95) Calcular a massa de gás hélio (peso molecular 4,0) contida num balão, sabendo-se que o gás ocupa um volume igual a 5,0 m3 e está a uma temperatura de -23 oC e a uma pressão de 30 cmHg.
a) 1,86 g
b) 46g
c) 96 g
d) 186 g
e) 385 g
96) 2,56.103 g de oxigênio, cuja molécula-grama é 32,0 g, ocupam 82,0 litros num recipiente à temperatura de – 23 oC. Sendo dado R = 0, 082 atm /mol.K, a pressão no interior do recipiente terá um valor de:
a) 200,0 atm
b) 20,0 atm
c) 0,2 atm
d) 0,02 atm
e) n.r.a.
97) Dois recipientes de mesmo volume estão ligados por um tubo de diâmetro pequeno provido de um registro (inicialmente fechado). O recipiente 1 contêm 4 mols de hidrogênio a 300 K. O recipiente 2 contém n mols do mesmo gás, à temperatura T. Assinale, entre as opções apresentadas, aquela que indica valores de n e T compatíveis com a seguinte observação experimental: "Ao abrir-se o registro, verifica-se um fluxo de gás do recipiente 1 para o 2".

98) Um cilindro de capacidade igual a 60 litros está cheio de oxigênio sob pressão de 9,2 atm à temperatura de 27 oC. Abre-se a válvula. Qual a massa de gás que escapa? Admite-se que a temperatura permanece constante e a pressão externa seja normal. (Para o oxigênio M = 32 g; R = 0,082 atm.l/mol.K)
a) 680 g
b) 560 g
c) 240 g
d) 640 g
e) 420 g
99) Reúnem-se, num recipiente de capacidade igual a 10 litros, 5 litros de hidrogênio à pressão de 20 atmosferas e 10 litros de oxigênio à pressão constante de 10 atmosferas. A pressão final da mistura, em atmosferas, é:
a) 10
b) 20
c) 15
d) 5
e) 30
100) A pressão que um gás exerce em uma superfície é devida:
a) ao choque entre as moléculas.
b) à força de atração entre as moléculas.
c) ao choque das moléculas contra a superfície considerada.
d) à força de repulsão entre as moléculas.
e) à força com que a superfície atrai as moléculas.
Gabarito


respostas bem práticas ajudaria muito :D
ResponderExcluirAlguem sabe a resposta da 92??
ResponderExcluiralguem sabe a 95 ?
ResponderExcluirAlguem sabe a 83?
ResponderExcluirEste comentário foi removido pelo autor.
ExcluirAlguem sabe a 85?
ResponderExcluir